„Bezpieczny” lek dla ciężarnych, który docierał także do Polski. Tysiące dzieci urodziło się okaleczonych
Talidomid to opowieść o epoce, w której wiara w „cudowną tabletkę” wyprzedziła naukę. Lek wprowadzony do obrotu bez odpowiednich badań nad wpływem na ciążę okazał się teratogenem — substancją zdolną uszkodzić rozwijający się płód. Dziś ta tragedia jest jednym z powodów, dla których procedury dopuszczania leków do obrotu wyglądają zupełnie inaczej.
"Cudowna" tabletka z lat 50.
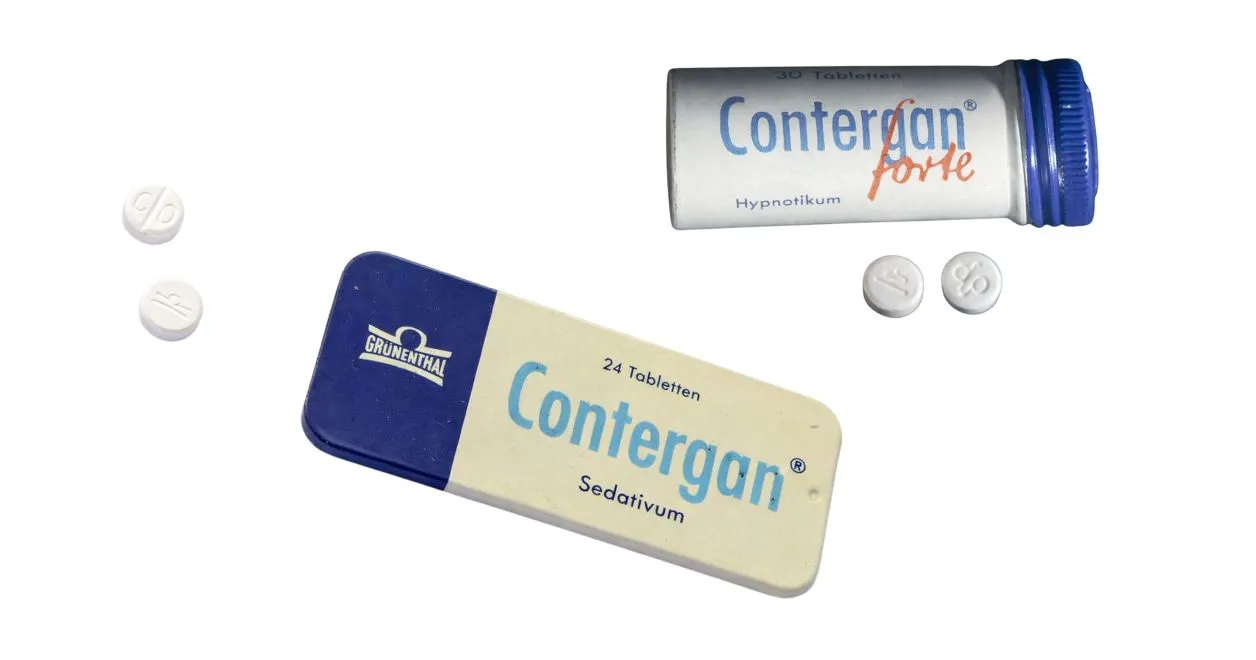
Talidomid trafił na rynek w 1957 roku dzięki niemieckiej firmie Grünenthal. W Niemczech sprzedawano go pod nazwą Contergan, a w materiałach reklamowych podkreślano „łagodność” i „nieszkodliwość” preparatu. Był środkiem uspokajającym i nasennym, polecanym także przy dolegliwościach ciążowych. Sprzedawano go w dziesiątkach krajów, często bez recepty. Hasło było proste: sen, spokój i bezpieczeństwo.
„Nieszkodliwy jak herbatnik z cukrem", tak reklamowano talidomid, zalecano go nawet dla niemowląt i małych dzieci – a także przeciwko mdłościom w ciąży. Lek i jego nieautoryzowane imitacje sprzedawano w około 70 krajach.
Problem polegał na tym, że nikt nie sprawdził, jak substancja wpływa na rozwijający się płód. W latach 50. nie istniały jeszcze obowiązkowe testy teratogenności. Talidomid przeszedł podstawowe badania toksykologiczne na dorosłych zwierzętach i to wystarczyło, by uznać go za „bezpieczny”.
Dzieci rodziły się z wadami, których wcześniej prawie nie widywano
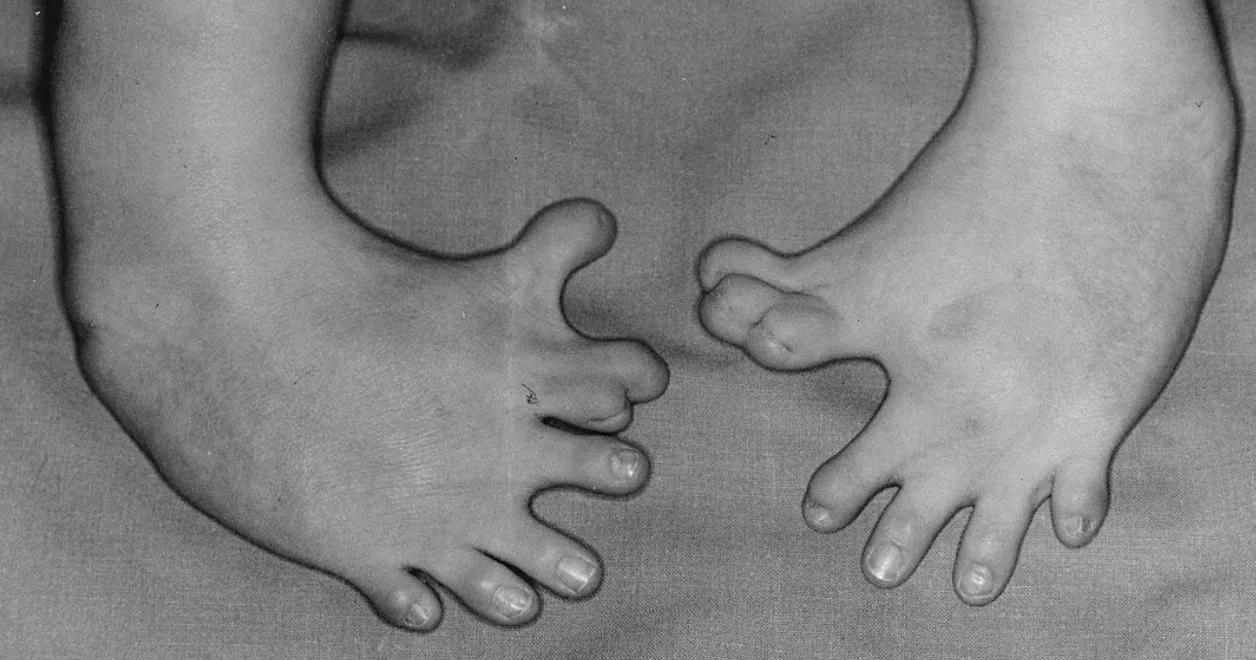
Pod koniec lat 50. lekarze zaczęli obserwować gwałtowny wzrost liczby noworodków z rzadkimi deformacjami: skróconymi ramionami, szczątkowymi dłońmi wyrastającymi z barków, brakiem nóg, a także wadami serca, nerek, słuchu i wzroku. Ten charakterystyczny obraz — zwłaszcza w odniesieniu do kończyn — kojarzony jest z fokomelią.
Z perspektywy czasu wiemy, że wystarczyła jedna tabletka w krytycznym momencie ciąży, by doszło do nieodwracalnych uszkodzeń. Szacunki różnią się w zależności od metod liczenia, ale globalnie mówi się o ponad 10 tysiącach dzieci dotkniętych ciężkimi wadami, z czego znaczna część nie przeżyła pierwszego roku życia.
Prawda wychodziła na jaw powoli. Jeszcze w 1960 roku pojawiały się pierwsze doniesienia o problemach neurologicznych u dorosłych pacjentów przyjmujących Contergan. Dopiero w 1961 roku niezależni lekarze powiązali wady wrodzone z talidomidem. Przełomem była publikacja prasowa w Welt am Sonntag z końca listopada 1961 roku, która jasno połączyła deformacje noworodków z „nieszkodliwym” środkiem nasennym. Wkrótce potem lek wycofano z rynku — ale było już za późno.
Embriopatia talidomidowa – oficjalna nazwa tragedii
W medycynie skutki działania talidomidu u płodu określa się jako embriopatię talidomidową. To zespół ciężkich wad wrodzonych powstających, gdy lek zostanie przyjęty między około 20. a 36. dniem ciąży – w kluczowym momencie formowania się kończyn i narządów.
Najczęściej obejmuje ona:
- skrócenie lub brak kończyn (fokomelię);
- deformacje dłoni i stóp;
- wady serca, nerek i przewodu pokarmowego;
- uszkodzenia słuchu i wzroku.
Mechanizm był szczególnie zdradliwy: lek nie powodował poronień w typowy sposób. Płód rozwijał się dalej – ale z nieodwracalnymi uszkodzeniami. To właśnie dlatego przez pewien czas nikt nie łączył tabletek uspokajających z dramatem rodzących się dzieci.
Dopiero analiza setek podobnych przypadków pozwoliła lekarzom zidentyfikować wspólne źródło.
Polska: „niezarejestrowany”, ale nieobecny tylko na papierze
W polskich opracowaniach podkreśla się, że talidomid nie został oficjalnie zarejestrowany w PRL. To prawda. Jednocześnie istnieją relacje i publikacje wskazujące, że lek był przywożony prywatnie — podobnie jak wiele zachodnich preparatów w tamtym okresie. Oznacza to, że mógł trafiać do obiegu poza formalną kontrolą.
W Polsce żyją osoby określane jako ofiary talidomidu. Jedna z opisywanych historii dotyczy mężczyzny urodzonego w latach 60., który — już jako dorosły — próbował dociec przyczyny swoich deformacji, łącząc je z lekami na mdłości przyjmowanymi przez matkę w ciąży. To niewygodna prawda o realiach tamtej epoki: brak rejestracji nie oznaczał braku kontaktu z produktem. Oznacza raczej, że nie ma pełnych danych, a wiele historii nie trafiło do oficjalnych statystyk, bo nie prowadzono wówczas systematycznych rejestrów wad wrodzonych.
Amerykański wyjątek
Jest jeden kraj, w którym katastrofę niemal całkowicie powstrzymano: Stany Zjednoczone. Stało się tak dzięki postawie Frances Oldham Kelsey, farmakolożki pracującej dla Food and Drug Administration. Kelsey odmówiła dopuszczenia talidomidu do sprzedaży, domagając się dodatkowych danych o bezpieczeństwie. Firma naciskała, dokumenty były niepełne — ona pozostała nieugięta.
Ta decyzja uchroniła tysiące amerykańskich dzieci przed losem, który spotkał ich rówieśników w Europie i Australii. To jeden z najdobitniejszych przykładów w historii farmakologii, jak wiele może zależeć od jednego urzędniczego „nie”.
Odpowiedzialność bez konsekwencji
Po wybuchu skandalu Grünenthal wypłaciła odszkodowania, ale przez dekady unikała jednoznacznego przyznania się do winy. Procesy ciągnęły się latami. Dopiero po ponad półwieczu firma wystosowała oficjalne przeprosiny.
Żaden z głównych decydentów nie trafił do więzienia.
Dla rodzin oznaczało to dożywotnią rehabilitację dzieci, protezy, kolejne operacje i życie z niepełnosprawnością spowodowaną tabletką reklamowaną jako „łagodna”.
Gdy dzieci dorosły
Niemieckie reportaże sprzed lat przypominają, że ta historia nie skończyła się w 1961 roku. Dorosłe dziś „dzieci talidomidowe” nadal zmagają się z powikłaniami: przewlekłym bólem, przeciążeniami kręgosłupa, problemami z protezami i zależnością od systemów wsparcia. Jedna z bohaterek takich reportaży urodziła się bez rąk i przez całe życie uczyła się funkcjonować w świecie zaprojektowanym dla ludzi w pełni sprawnych.
To ważne, bo pokazuje skalę: talidomid nie tylko okaleczył ciała — ukształtował całe biografie.
Co ta tragedia zmieniła na zawsze
Skandal talidomidowy stał się impulsem do globalnej reformy prawa farmaceutycznego. Wprowadzono obowiązkowe wieloetapowe badania kliniczne, testy wpływu na rozwój embrionalny, rygorystyczne procedury rejestracyjne i systemy raportowania działań niepożądanych.
To nie jest tylko historia „złego leku”. To historia o tym, jak reklama i wiara w postęp potrafią wyprzedzić dowody. Wystarczyło kilka lat, by okazało się, że prostota była złudzeniem — a koszt poniosły dzieci.
W polskim kontekście dochodzi jeszcze jedna lekcja: nawet jeśli coś „formalnie nie istniało” w systemie, mogło istnieć w praktyce. I dlatego w tej opowieści Polska nie jest tylko widzem.
Bibliografia
- Rehman W., Arfons J., The Rise, Fall and Subsequent Triumph of Thalidomide, Journal of Oncology Pharmacy Practice (2011).
- Materiały historyczne firmy Grünenthal – wprowadzenie leku w 1957 r., wycofanie w 1961 r.
- Opracowania nt. katastrofy Conterganu i publikacje Welt am Sonntag (1961) – chronologia ujawnienia związku między lekiem a wadami wrodzonymi.
- Biogram Frances Oldham Kelsey – U.S. National Library of Medicine.
- Przeglądy naukowe dotyczące liczby poszkodowanych i mechanizmu teratogenności talidomidu (m.in. PMC).
- Polskie publikacje popularnonaukowe (Medonet, „Gazeta Wyborcza”) dotyczące braku rejestracji w PRL oraz prywatnego napływu leku do Polski i relacji polskich ofiar.